Клиническая эффективность нового шампуня на основе комбинации циклопироксоламин/пиритион цинка в лечении себорейного дерматита кожи головы
Группа исследователей:
1. Госпиталь Труссо, Отделение дерматологии, 37044 Тур Седекс 01, Франция
2. Исследовательский институт Пьера Фарбра, Технологический парк канала, 4 рю Мари
Кюри, п/я 33132, 31521, Рамонвиль, Франция
3. Франция: Michele Decuyper, MD; Yolaine Farcet, MD; Marie-Laure Flechet, MD;
Jean-Luc Haziza, MD; Mireille Ruer-Mulard, MD; Jean-Paul Poirier, MD; Jean-Marc Durand, MD;
Marie-Helene Garnier–Calas, MD; Marie-Christine Pouget, MD; Michel Weiller, MD
Tunisia: Rafia Nouira, MD, phD; Nejib Doss, MD, phD; Amel Ben Osman, MD, phD;
Ridha Kamoun, MD, phD; Insaf Mokthar, MD, phD
Активные противогрибковые вещества циклопироксоламин (ЦПО) и пиритион цинка (ПЦ) эффективны в лечении себорейного дерматита кожи головы. Данное многоцентровое простое слепое клиническое исследование проводилось с целью оценить эффективность шампуня, в состав которого входит комбинация 1,5% раствор ЦПО/1% раствор ПЦ, в сравнении с шампунем с инертной основой и пенящимся гелем, содержащим 2% кетоконазола, в лечении себорейного дерматита. У 189 больных, рандомизированно распределенных в группы применения одного из трех препаратов (дважды в неделю в течение 28 дней), в нулевой день, а также на 7-й, 14-й и 28-й день измерялись следующие параметры: общий показатель поражения кожи, степень выраженности эритемы и зуда, общая эффективность испытуемых продуктов, качество жизни (опросники SF‑12 и DLQI — Индекс качества жизни при заболеваниях кожи) и переносимость.
Все три продукта снизили выраженность общей симптоматики, эритемы и зуда начиная с 7-го дня (р < 0,0001). Два противогрибковых средства на 14-й день были статистически значимо более эффективными в плане снижения показателя степени тяжести, поражения, симптомов эритемы и зуда, чем шампунь с инертной основой (р < 0,0001). На 7-й день шампунь на основе комбинации ЦПО/ПЦ показал большую эффективность в снижении выраженность симптомов зуда, чем гель, содержащий кетоконазол, и шампунь с инертной основой (р = 0,032 и р < 0,001 соответственно).
Общая эффективность двух противогрибковых средств, которая на 28-й день оценивалась исследователем и больным, была статистически значимо лучше, чем таковая шампуня с инертной основой. По всем пунктам опросника DLQI улучшение наблюдалось только в группе применения шампуня на основе комбинации ЦПО/ПЦ. В лечении СД шампунь на основе комбинации ЦПО/ПЦ продемонстрировал такую же быстроту действия и эффективность, как гель с содержанием кетоконазола.
Себорейный дерматит является распространенным хроническим заболеванием кожи, которым страдают 3–5% взрослого населения [1, 2]. Дрожжевые грибы рода Malassezia, которые повсеместно встречаются как часть условной патогенной микрофлоры кожи, могут быть важным фактором развития данного заболевания, так как у больных себорейным дерматитом (или перхотью — его легкой формой) они обнаруживаются в большем количестве, чем у здоровых людей [3–7]. Штаммы дрожжевых грибов Malassezia Restricta и Malassezia Globosa, по всей видимости, чаще всего встречаются при заболеваниях [3, 8, 9], но также отмечались случаи СД, когда превалировали Malassezia Furfur, Malassezia Sympodialis и Malassezia Obtusa [4, 7]. Их этиологическая роль в развитии себорейного дерматита подтверждается несколькими исследованиями, в ходе которых была продемонстрирована эффективность противогрибковых препаратов для наружного применения в плане улучшения показателей клинического поражения и увеличение периода ремиссии [10–14], в основном за счет уменьшения количества грибковых клеток рода Malassezia [15–17].
Применение в комплексных методах лечения с кератолитическим действием или кортикостероидными препаратами для наружного применения в комбинации с противогрибковыми средствами, тестированных на предмет потенциального синергического дополняющего действия компонентов, также подтвердил их эффективность [13, 17, 18]. В связи с этим на основании специфических свойств этих двух компонентов была пред-
ложена новая комбинация: циклопироксоламин (ЦПО) и пиритион цинка (ПЦ).
ЦПО является противогрибковым препаратом широкого спектра действия, который также оказывает противовоспалительное действие за счет ингибирования синтеза простагландинов и лейкотриенов [19, 20]. Его эффективность в лечении себорейного дерматита и перхоти была продемонстрирована в ходе нескольких рандомизированных контролируемых исследований, но особенно высокую эффективность ЦПО демонстрировал в концентрации 1% [14, 21, 22] и 1,5% [12, 23] или в комбинации с другим противогрибковым препаратом [13].
Что касается ПЦ, он известен тем, что проявляет как неспецифическую кератолитическую, так и противогрибковую активность [24, 25], и эффективен в лечении себорейного дерматита и перхоти [26] в основном за счет того, что нормализует измененную ультраструктуру рогового слоя, которая наблюдается при перхоти [27]. Комбинация 1,5% ЦПО/1% ПЦ была исследована in vitro на двух штаммах дрожжевых грибов рода Malassezia (Malassezia globosa и Malassezia restricta) и продемонстрировала синергическое ингибиторное и фунгицидное действие с более высокой эффективностью в сравнении с 2% кетоконазолом (Panizzotti C, представлено к публикации). Предварительное клиническое исследование также продемонстрировало эффективность комбинации ЦПО/ПЦ в плане уменьшения площади поражения и степени тяжести клинической симптоматики у 11 больных, страдающих себорейным дерматитом.
Цель данного исследования – подтвердить эти предварительные результаты и оценить клиническую эффективность одномесячного лечения шампунем, содержащим комбинацию 1,5% ЦПО/1% ПЦ в сравнении с пенящимся гелем с 2% содержанием кетоконазола и шампунем с инертной основой ЦПО/ПЦ на большом количестве больных с себорейным дерматитом кожи головы средней или высокой степени тяжести.
Пациенты и методы
Дизайн исследования
Данное многоцентровое, контролируемое, простое слепое, рандомизированное клиническое исследование разработано для сравнения результатов лечения больных в трех параллельных группах и проводилось с января по июль 2004 года шестнадцатью дерматологами, одиннадцать из которых работали во Франции, а пятеро — в Тунисе. Исследование проводилось после утверждения протокола исследования независимым этическим комитетом города Тур во Франции в соответствии с этическими принципами, установленными Хельсинкской декларацией, и местными законодательными требованиями каждой страны.
Обследуемая группа больных
Критерии включения
Французские и тунисские дерматологи включили в исследование больных мужского и женского пола в возрасте от 18 лет и старше с клинически диагностированным себорейным дерматитом кожи головы, при наличии шелушения кожи головы, эритемы и зуда и с общим показателем поражения ≥ 36 по шкале, приведенной у Squire et al. [13]. Перед началом исследования все участники исследования подписали письменное информированное согласие.
Критерии исключения
В исследование не были включены больные с себорейным дерматитом с показателем поражения < 36 или требующие сопутствующего лечения кортикостероидными препаратами, а также больные с диагностированной аллергией на один из испытуемых продуктов.
Также в исследование не были включены больные, которым требовалось системное лечение антибиотиками, противогрибковыми или кортикостероидными препаратами; больные, которые уже использовали кортикостероиды местного применения, ретиноиды или антибиотики и противогрибковые препараты для местного применения или приема внутрь не ранее чем за неделю до визита включения; больные, которые использовали кортикостероидные препараты для приема внутрь или ретиноиды не ранее чем за 14 дней и 3 месяца соответственно перед визитом включения.
Также из исследования были исключены больные, которые не могли совмещать свое участие в другом исследовании с участием в данном исследовании или которые на тот момент уже участвовали в другом исследовании; беременные или кормящие грудью женщины, больные с иммунодефицитом и больные с дерматозом кожи головы, а также больные, которые на момент включения принимали препараты, способные повлиять на оценку себорейного дерматита.
Схема лечения
Для раздачи больным, случайным образом распределенным в три параллельные группы, три продукта были приготовлены, упакованы, промаркированы и пронумерованы согласно машинному списку рандомизации, установленному аналитиком биостатистики, который был назначен спонсором исследования. Больные получили бутылку с номером, соответствовавшим их номеру включения, которая содержала либо шампунь с комбинацией 1,5% ЦПО/1% ПЦ (Kelual DSTM, «Пьер Фабр»), либо пенящийся гель с 2% содержанием кетоконазола (Ketoderm®, «Янсен Силаг»), либо шампунь с с инертной основой без противогрибкового действия. Так как все три средства было легко отличить друг от друга по внешнему виду, исследование было запланировано как простое слепое: для того чтобы исследователи не знали о применяемом лекарственном средстве в данной группе, все три продукта были упакованы в одинаковые бутылки из темного стекла объемом 200 мл. На визите включения больные получили по одному флакону шампуня и инструкцию по его применению: 2 раза в неделю, 28 дней. Больные были проинструктированы о том, что в течение первых двух часов после применения тестируемого продукта и в дни визитов им нельзя наносить на кожу головы другие вещества. Больных также попросили с определенной частотой записывать в их дневниках все изменения и способ применения продукта и на последнем визите вернуть использованную бутылку исследователю, который должен был определить оставшееся количество продукта (полная, частично использованная или пустая). Любое лечение, которое могло повлиять на оценку пользы тестируемых средств, например, перманентная завивка и окрашивание волос, использование других шампуней помимо тестируемых продуктов, системное или местное применение антибиотиков, противогрибковых препаратов, кортикостероидов или ретиноидов или какого-либо другого местного лечения себорейного дерматита, было категорически запрещено в течение всего периода исследования.
Критерии оценки
Основной критерий эффективности
Основной критерий эффективности оценивался по шкале, отражающей степень поражения в нулевой день (Д0), на 7-й день (Д7), 14-й день (Д14) и 28-й день (Д28), через два дня после последнего применения шампуня. Показатель поражения определялся по шкале от 0 до 80 и учитывал площадь кожного покрова, пораженного себорейным дерматитом, и по степени тяжести поражения как описано у Squire et al. [13].
Вторичные критерии
Клинические симптомы
Степень тяжести эритемы и зуд определялись исследователем в нулевой день, на 7-й, 14-й и 28-й день по шкале из трех пунктов: от 0 (отсутствие) до 3 (тяжелая степень).
Общая оценка эффективности исследователями и больными
На визите завершения (28-й день) общая эффективность лечения определялась исследователем по общей выраженности симптоматики: ухудшение — 0, стагнация — 1, умеренное улучшение — 2, ярко выраженное улучшение — 3 и выздоровление — 4; и пациентом по шкале из пяти пунктов: от 0 (абсолютно не доволен) до 4 (очень доволен).
Качество жизни
Влияние лечения на качество жизни пациента оценивалось при помощи двух опросников, которые заполнялись пациентом в начале (нулевой день) и в конце исследования (28-й день). Первый опросник был утвержденной во Франции стандартной версией SF‑12 [28], который повсеместно используется для оценки общего состояния здоровья. Чем ниже показатель, тем больше влияние лечения на качество жизни. При помощи второго опросника измеряется качество жизни пациентов с кожными заболеваниями. С согласия автора, утвержденный опросник из 10 пунктов DLQI (Индекс качества жизни при заболеваниях кожи) [29] был адаптирован специально для заболеваний кожи головы путем простой замены слова «кожа» на словосочетание «кожа головы» в каждом вопросе. Каждый пункт оценивался по 4-балльной шкале от 0 (совсем нет) до 3 (очень). Общий показатель вычислялся путем сложения всех показателей по каждому пункту и составлял от 0 до 30 баллов. Чем выше был общий показатель, тем ниже оценивалось качество жизни. Если на 1 из пунктов пациент не давал ответа, его считали за 0. Если пациент пропускал более одного вопроса, его анкета DLQI исключалась из анализа.
Местная переносимость
Местная переносимость оценивалась исследователем при каждом посещении доктора, которые следовали после визита включения. В случае развития нежелательного явления больной извещал исследователя о его продолжительности, степени тяжести и последствиях, затем исследователь регистрировал обнаруженное нежелательное явление. О развитии тяжелых нежелательных явлений исследователи должны были докладывать спонсору в течение двух дней после регистрации данного нежелательного явления исследователем.
Статистические методы
Статистический анализ производился с использованием программного обеспечения SAS, версия 8.2.
Все количественные критерии вычислялись и выражались при помощи следующих характеристик: размер образца, среднее значение, стандартная погрешность (СП), медианное значение и диапазон; качественные критерии выражались в процентном отношении и частоте.
В нулевой день сравнение между тремя группами проводилось по количественным критериям с использованием дисперсионного анализа с нормальным распределением или же теста Крускала – Уоллиса. Для оценки размера образцов < 5 по качественному критерию использовался критерий хи-квадрат или точный критерий Фишера, а для оценки образцов > 4 — тест Крускала – Уоллиса.
Внутригрупповой анализ влияния времени на действие продукта проводился при помощи дисперсионного анализа с парным сравнением при помощи теста Стьюдента или Вилкоксона. Для анализа качественных переменных использовался тест Мак-Немара на серии отличий. Межгрупповой анализ проводился при помощи дисперсионного анализа с нормальным распределением или же теста Крускала – Уоллиса. Все статистические тесты были двусторонними и проводились при показателе статистической значимости 0,05.
Результаты
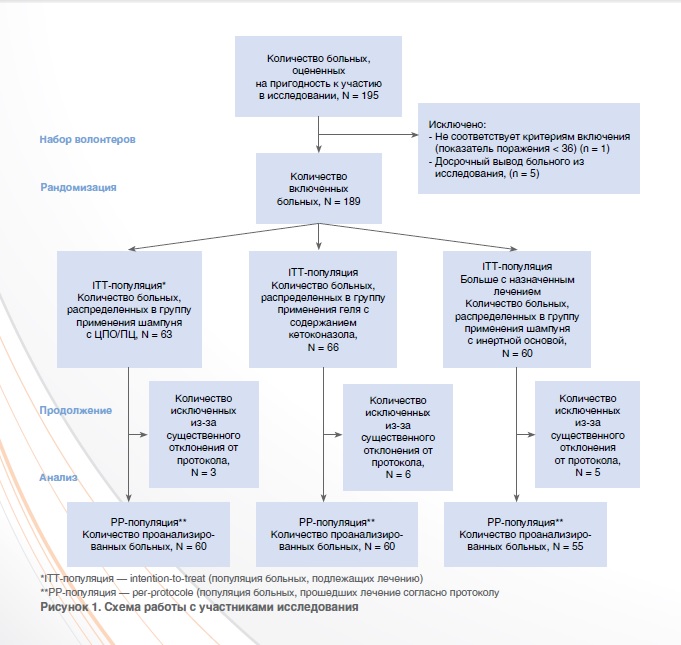
Весь контингент участников исследования представлен на рисунке 1. В общей сложности в группу ITT-популяции было включено 189 больных. Согласно рандомизации, 63 больных получали лечение шампунем на основе комбинации ЦПО/ПЦ, 66 больных получали лечение пенящимся гелем с содержанием кетоконазола и 60 больных применяли шампунь с инертной основой. Результаты четырнадцати больных были исключены из анализа результатов по протоколу (РР) из-за существенных отклонений от него. Так как по РР-популяции в основном были получены схожие результаты, на схеме приведены результаты по ITT-популяции в тех случаях, когда нет уточнения по РР-популяции.
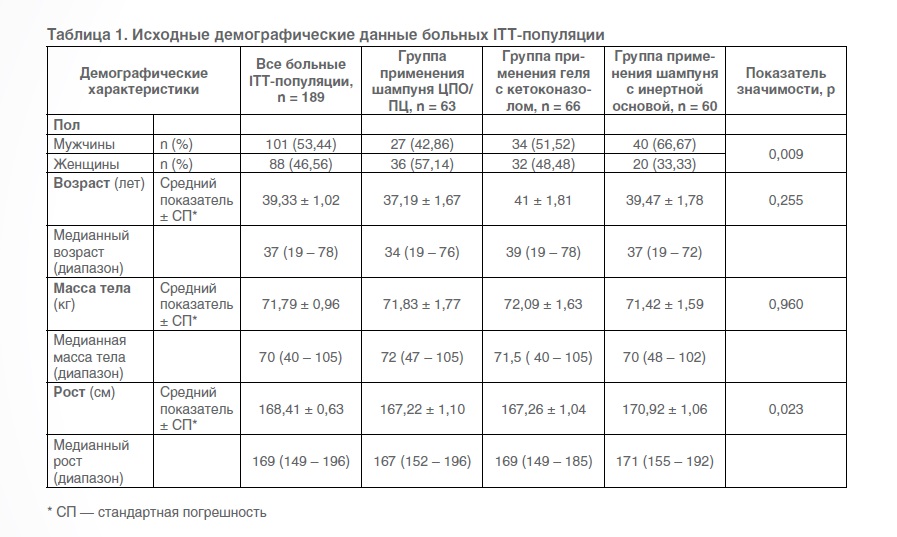
Демографические данные и исходные клинические характеристики
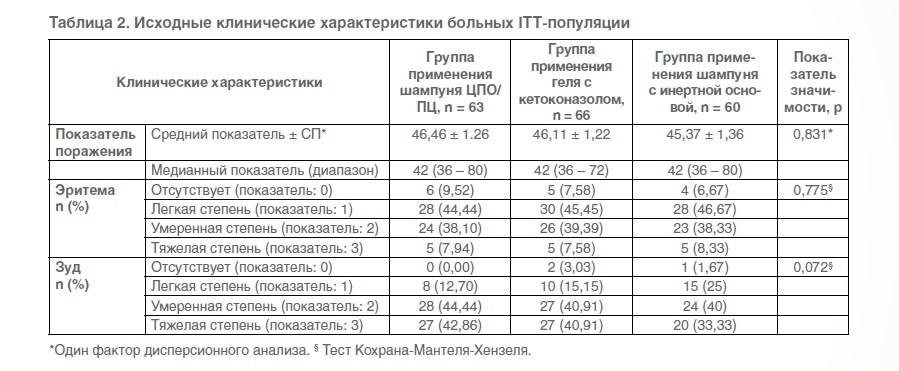
Демографические данные и исходные клинические характеристики больных представлены на рисунке 1. В ITT-популяцию входили 101 мужчина и 88 женщин, средний возраст которых составлял 39,33 ± 1,02 года (19–78 лет). На визите включения в исследование статистически значимой разницы в демографических данных между группами не наблюдалось, за исключением роста больных (в группе применения шампуня с инертной основой рост больных был статистически значимо ниже, чем в других группах) и соотношения полов (статистически значимая разница между группами).
Что касается клинических критериев включения, статистически значимой разницы в плане показателя поражения (р = 0,831), симптомов эритемы (р = 0,755) и зуда (р = 0,072) между тремя группами не наблюдалось (рисунок 2).
Основной критерий оценки
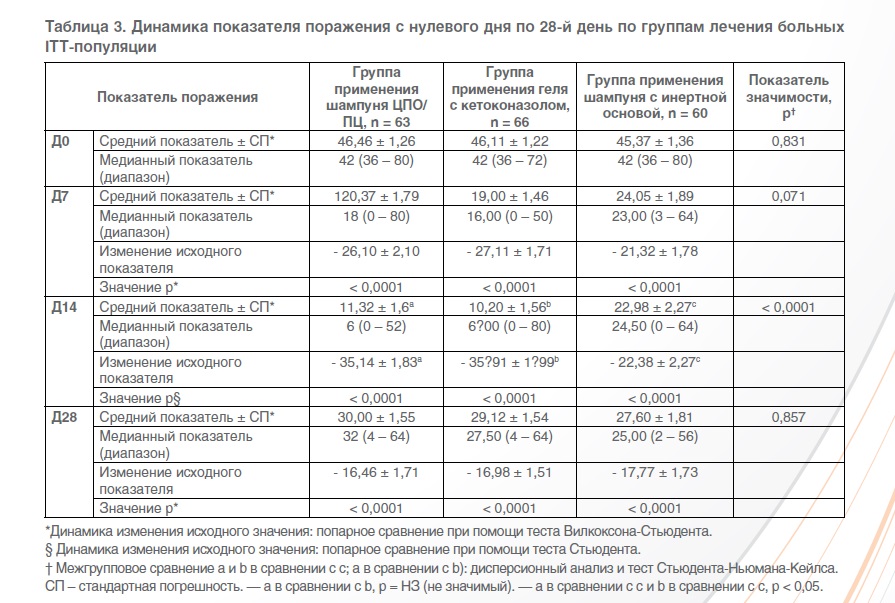
В трех группах лечения на каждом исследовательском визите, начиная с визита включения, наблюдалось значительное статистически значимое улучшение среднего показателя поражения (р < 0,0001) (таблица 3). На каждом исследовательском визите в обеих группах применения лечебных шампуней (на основе комбинации ЦПО/ПЦ и с содержанием кетоконазола) наблюдалось снижение показателя поражения без статистически значимой разницы между двумя группами. В сравнении с шампунем с инертной основой снижение показателя поражения было более значительным в группах применения обоих противогрибковых средств, со статистически незначимой разницей на 7-й день (р = 0,071) и большой статистически значимой разницей на 14-й день (р < 0,0001). На 28-й день, напротив, никакой статистически значимой разницы между тремя группами в плане снижения показателя поражения по сравнению с исходным показателем не наблюдалось: -16,46 ± 1,71 в группе применения шампуня на основе комбинации ЦПО/ПЦ, -16,98 ± 1,51 в группе применения геля с содержанием кетоконазола и -17,77 ± 1,73 в группе применения шампуня с инертной основой (р = 0,857).
При анализе РР-популяции в основном, были получены аналогичные результаты, однако на 7-й день была достигнута статистически значимая разница в показателях поражения в сравнении с шампунем с инертной основой в пользу двух противогрибковых средств (р = 0,046).
Дополнительные критерии оценки
Клинические симптомы
Результаты оценки динамики симптомов эритемы и зуда в течение лечения приведены в таблицах 2 и 3 соответственно.
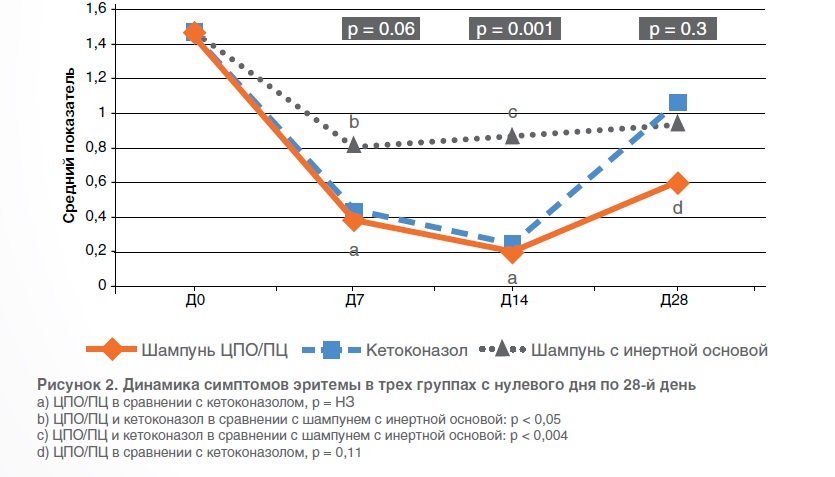
Эритема
Начиная с 7-го дня и затем на каждом исследовательском визите отмечалось ярко выраженное и значительное статистически значимое уменьшение выраженность эритемы (р < 0,0001), самое значительное улучшение наблюдалось на 14-й день, после чего, на 28-й день, отмечался небольшой спад, однако при этом показатели эритемы оставались намного более низкими, чем значения, отмеченные в нулевой день.
При сравнении результатов в двух группах применения противогрибковых средств на 7-й и 14-й день было выявлено одинаковое улучшение без статистически значимой разницы между группами применения СПО/ПЦ и кетоконазола (р = 0,992 и р = 0,954 соответственно), тогда как на 28-й день отмечалась небольшая разница в пользу шампуня на основе комбинации ЦПО/ПЦ, однако разница не была статистически значимой (р = 0,015). Шампунь с инертной основой на всех визитах после нулевого дня (на 7-й и 14-й день), за исключением 28-го дня, напротив, обладал более низкой эффективностью, чем два противогрибковых средства, со статистически значимой разницей между шампунем с инертной основой и шампунем на основе комбинации ЦПО/ПЦ и гелем с содержанием кетоконазола на 7-й день: р = 0,041 и р = 0,046 соответственно, на 14-й день: р = 0,003 и р = 0,001 соответственно, и статистически незначимой разницей на 28-й день: р = 0,443 и р = 0,478 соответственно.
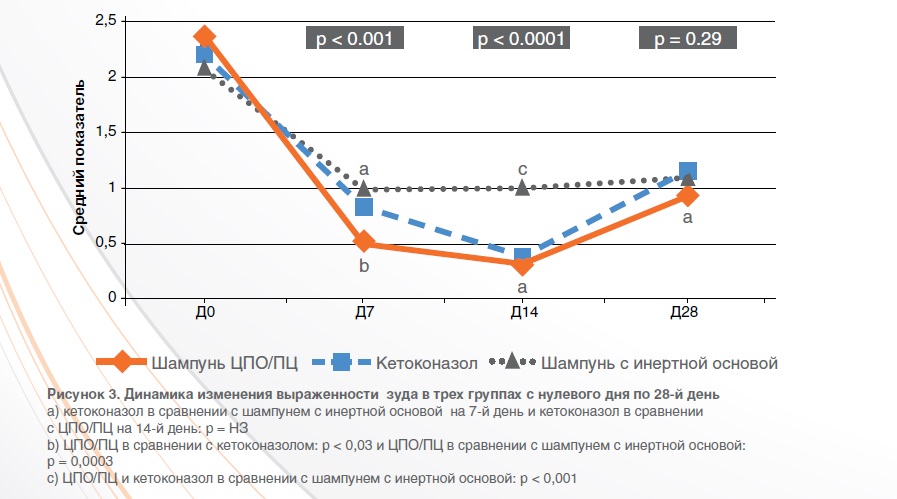
Зуд
Такая же картина наблюдалась в отношении показателей зуда, которые на 7-й день начали резко улучшаться во всех трех группах и сохраняли эту динамику на протяжении всего периода исследования, с небольшим спадом на 28-й день в группах применения шампуня на основе комбинации ЦПО/ПЦ и геля с содержанием кетоконазола. Самая высокая эффективность лечения наблюдалась на 7-й день в группе применения шампуня на основе комбинации ЦПО/ПЦ, который вызвал более значительное статистически значимое снижение интенсивности зуда, чем гель с содержанием кетоконазола и шампунь с инертной основой (р = 0,032 и р < 0,001 соответственно), которые произвели такое же действие (р = 0,133). На 14-й день гель с содержанием кетоконазола демонстрировал такую же эффективность, как и шампунь на основе комбинации ЦПО/ПЦ (р = 0,365), оба вышеуказанных противогрибковых средства были более эффективными, чем шампунь с инертной основой (р = 0,002 и р = 0,0001 соответственно), тогда как на 28-й день разница в результатах была незначительная.
Общая эффективность
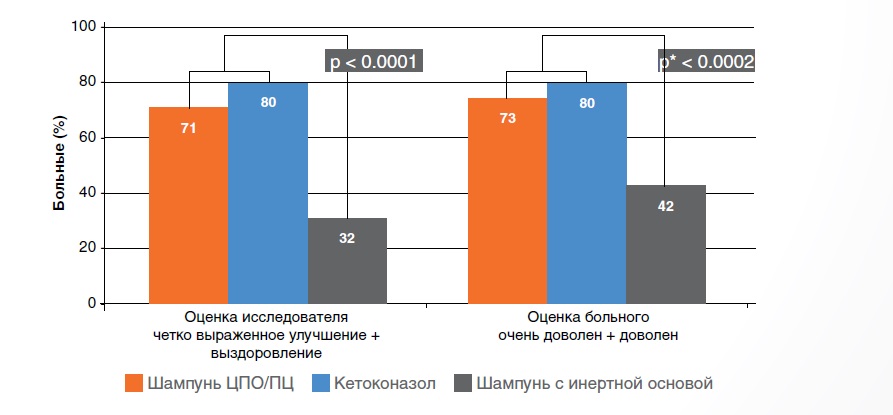
Результаты оценки общей эффективности (оценка производилась исследователем и больным) представлены в таблице 4.
Оценка исследователя
По оценке исследователя, оба противогрибковых средства, шампунь на основе комбинации ЦПО/ПЦ и гель с содержанием кетоконазола, продемонстрировали одинаковую эффективность (р = 0,557) с улучшением или выздоровлением у 71 и 80% больных соответственно и оказались статистически значимо более эффективными, чем шампунь с инертной основой (р < 0,0001), в плане уменьшения или устранения симптомов себорейного дерматита.
Оценка больного
Аналогичная картина наблюдается в отношении мнения больных: 73 и 80% больных, соответственно получавших лечение шампунем на основе комбинации ЦПО/ПЦ и гелем с содержанием кетоконазола, указали, что они «довольны» или «очень довольны», по сравнению с 42% больных из группы применения шампуня с инертной основой (р < 0,0002).
Переносимость
Шампунь на основе комбинации ЦПО/ПЦ, гель с содержанием кетоконазола и шампунь с инертной основой переносились одинаково хорошо: 96,7, 98,4 и 94,9% больных отметили переносимость лечебных средств как «хорошо» или «очень хорошо» (р = 0,360).
Нежелательные явления легкой и умеренной степени отмечались у 12 больных: 5 — в группе применения шампуня с ЦПО/ПЦ, 3 — в группе применения геля с кетоконазолом и 4 — в группе применения шампуня с инертной основой. Наиболее распространенными нежелательными явлениями были эритема и ощущение жжения, которые, возможно, могли быть связаны с применением тестируемого продукта, но при этом не требовали прекращения лечения и в половине случаев спонтанно исчезали.
Качество жизни
Для статистического анализа качества жизни использовались результаты только тех больных, у которых на визите включения и на 28-й день были пригодные для анализа показатели. Поэтому для оценки общего состояния здоровья были проанализированы показатели 140 больных (опросник SF‑12), а для оценки состояния кожи головы — показатели 169 больных (адаптированный опросник DLQI).
Опросник SF‑12 заполнили 47 больных из группы применения шампуня на основе комбинации ЦПО/ПЦ, 49 больных из группы применения геля с кетоконазолом и 44 больных из группы применения шампуня с инертной основой. В моральном и физическом отношении показатели были сравнимы с таковыми, полученными на визите включения (р = 0,979 и р = 0,354 соответственно). При сравнении динамики между нулевым и 28-м днями ни один из трех продуктов не продемонстрировал статистически значимого улучшения в плане пока-
зателей умственного или физического состояния. Кроме того, сравнение между тремя продуктами в плане среднего показателя физического и умственного состояния не выявило какой-либо статистически значимой разницы (р = 0,238 и р = 0,780 соответственно).
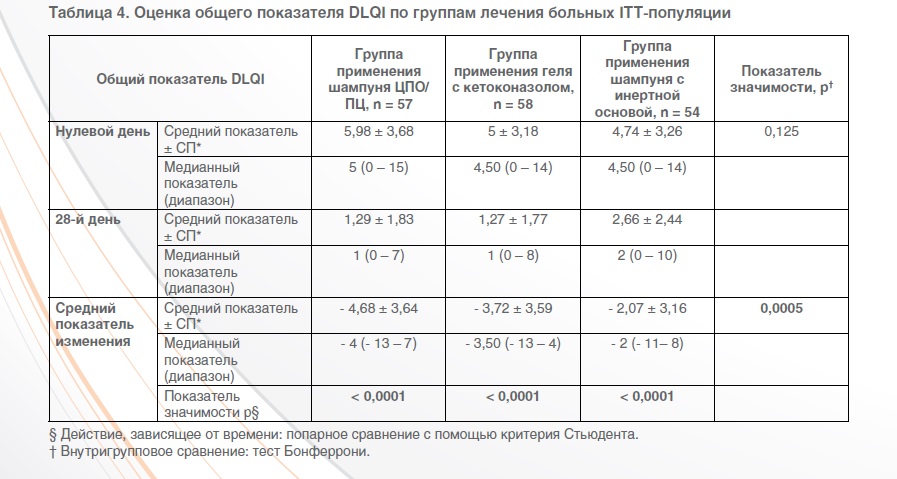
Для анализа по опроснику DLQI (таблица 4) использовались показатели 57 больных из группы применения шампуня на основе комбинации ЦПО/ПЦ, 58 больных из группы применения геля с кетоконазолом и 54 больных из группы применения шампуня с инертной основой. Показатели DLQI были сравнимы с таковыми, полученными на визите включения. На 28-й день в трех группах показатели опросника DLQI статистически значимо улучшились, но в группах применения шампуня с комбинацией ЦПО/ПЦ и геля с кетоконозолом это улучшение
было более значительным, чем в группе применения шампуня с инертной основой, со средним увеличением общего среднего показателя DLQI на 4,68 и 3,72 пункта соответственно в сравнении с 2,07 пунктами (р < 0,05 в обеих группах).
Также был проведен анализ показателей DLQI на основании результатов измерений. Только шампунь на основе комбинации ЦПО/ПЦ вызвал статистически значимое улучшение в сравнении с исходными показателями для шести измерений (р < 0,05 у всех больных). Показатели измерений «работа» и «лечение», как и показатели измерений «отдых» и «лечение», не продемонстрировали статистически значимого улучшения ни в группе
применения геля с кетоконазолом (р = 0,051 и р = 1,00 соответственно), ни в группе применения шампуня с инертной основой (р = 0,067 и р = 0,766 соответственно).
Обсуждение
Данное рандомизированное простое слепое клиническое исследование наглядно продемонстрировало эффективность шампуня на основе комбинации 1,5% ЦПО/1% ПЦ в лечении себорейного дерматита кожи головы. С первой недели лечения и в течение всего периода лечения шампунь на основе комбинации ЦПО/ПЦ обеспечивал значительное статистически значимое уменьшение зоны распространения и интенсивности
шелушения, которые измерялись при помощи показателя поражения, а также симптомов эритемы и зуда, обусловленных данным заболеванием.
Межгрупповой анализ на 7-й и 14-й день продемонстрировал более высокую эффективность шампуня с ЦПО/ПЦ и геля с кетоконазолом в сравнении с шампунем с инертной основой, при этом эффективность обоих противогрибковых средств возрастала со временем. Действие шампуня с инертной основой, который также тестировался в ходе других исследований [12, 14, 30, 31], на 7-й и 14-й день хотя и являлось статистически значимым, было намного слабее, чем таковое двух других продуктов.
Кроме того, шампунь с ЦПО/ПЦ продемонстрировал эффективность, сравнимую с таковой пенящегося геля с содержанием кетоконазола, так как на всех визитах между двумя продуктами не наблюдалось никакой статистически значимой разницы в плане улучшения показателя поражения и уменьшения выраженности эритемы. Однако необходимо отметить, что в отношении зуда шампунь с ЦПО/ПЦ, по всей видимости, действует быстрее и эффективнее, чем гель с кетоконазолом, так как на 7-й день он вызывал более значительное статистически значимое уменьшение зуда, на который, как правило, прежде всего жалуются больные. Это быстрое и ярко выраженное действие может быть обусловлено присутствием в составе шампуня такого компонента, как ЦПО, который в другом исследовании уже продемонстрировал свою более высокую эффективность в плане общего уменьшения зуда кожи головы [13]. Однако его преимущество по данному критерию в сравнении с кетоконазолом требует подтверждения, так как ни в одном из этих исследований оно не анализировалось [12, 32].
Эффективность трех продуктов, хотя и оставалось все время статистически значимо высокой, немного снизилась к концу исследования. Так, при обследовании на 28-й день в трех группах лечения наблюдалось увеличение показателя поражения без статистически значимой разницы между группами, что указывало на незначительный рецидив болезни в исследуемой популяции. Если в группе применения шампуня с инертной основой на 14-й и 28-й день улучшение показателей эритемы и зуда было абсолютно одинаковым, то в группах применения шампуня с ПЦО/ЦП и геля с кетоконазолом на 28-й день оно снизилось до уровня, достигнутого шампунем с инертной основой.
Данные результаты не согласуются с таковыми, полученными в других сравнительных исследованиях, в ходе которых оценивалась эффективность кетоконазола [12, 30, 31, 33] и ЦПО в отдельности [21–23] и в комбинации [13]. Во всех этих исследованиях пенящийся гель с кетоконазолом и ЦПО на протяжении всего периода четырехнедельного исследования оказывали стабильное ярко выраженное действие на себорейный дерматит, которое сохранялось до момента оценки возможного рецидива в течение периода наблюдения после
завершения лечения [12, 33].
Несоответствие результатов может объясняться недостаточной приверженностью субъектов протоколу лечения в конце исследования. Из-за быстрого и ярко выраженного улучшения, наступающего после первых двух недель лечения благодаря применению обоих противогрибковых шампуней, многие больные могли решить, что больше нет необходимости продолжать лечение до конца исследования, и не так строго придерживались инструкций по применению исследуемого продукта.
Кроме того, несмотря на то, что на 28-й день показатели поражения снова были повышенными, они все же оставались статистически значимо ниже исходных значений. По оценке и больных, и исследователей, была отмечена значительная статистически значимая большая эффективность у 2-х активных шампуней по сравнению с шампунем с инертной основой. Около 75% больных указали, что они были «довольны» и «очень довольны» своим лечением комбинацией ЦПО/ПЦ или кетоконазолом.
Принимая во внимание дополняющие фунгицидные и фунгистатические свойства ЦПО и ПЦ, которые наблюдались в in vitro исследованиях, и продемонстрированную клиническую эффективность комбинации ЦПО/ПЦ в составе шампуня для лечения средней и тяжелой степени себорейного дерматита, необходимо провести дальнейшие более продолжительные исследования для оценки его остаточного действия после завершения лечения.
Источник: Eur J Dermatol 2006; 16 (5): 558–564
Ссылки
1. Johnson M-L, Roberts J. Prevalence of dermatological diseases among persons 1–74 years of age: United States. Advance data report No. 4. U.S. Department of Health, Education, and Welfare, 1977.
2. Gupta AK, Madzia SE, Batra R. Etiology and management of Seborrheic dermatitis. Dermatology. 2004; 208: 89–93.
3. Gupta AK, Batra R, Bluhm R, et al. Skin diseases associated with Malassezia species. J Am Acad Dermatol. 2004; 51: 785–798.
4. Nakabayashi A, Sei Y, Guillot J. Identification of Malassezia species isolated from patients with seborrhoeic dermatitis, atopic dermatitis, pityriasis versicolor and normal subjects. Med Mycol. 2000; 38: 337–341.
5. Heng MC, Henderson CL, Barker DC, Haberfelde G. Correlation of Pityrosporum ovale density with clinical severity of seborrheic dermatitis as assessed by a simplified technique. J Am Acad Dermatol. 1990; 23: 82–86.
6. Groisser D, Bottone EJ, Lebwohl M. Association of Pityrosporum orbiculare (Malassezia furfur) with seborrhoeic dermatitis in patients with acquired immunodeficiency syndrome (AIDS). J Am Acad Dermatol. 1989; 20: 770–773.
7. Sandstrem Falk M-H, Tengvall Linder M, Johansson C, et al. The prevalence of Malassezia Yeasts in patients with atopic dermatitis, seborrhoeic dermatitis and healthy controls. Acta Derm Venereol. 2005; 85: 17–23.
8. Gupta AK, Kohli Y, Summerbell RC, Faergemann J. Quantitative culture of Malassezia species from different body sites of individuals with or without dermatoses. Med Mycol 2001; 39: 243–251.
9. Gemmer CM, DeAngelis YM, Theelen B, et al. Fast, noninvasive method for molecular detection and differentiation of Malassezia yeast species on human skin and application of the method to dandruff microbiology. J Clin Microbiol. 2002; 40: 3350–3357.
10. Ford GP, Farr PM, Ive FA, Shuster S. The response of seborrhoeic dermatitis to ketoconazole. Br J Dermatol. 1984; 111: 603–607.
11. Ortonne JP, Lacour JP, Vitetta A, Le Fichoux Y. Comparative study of ketoconazole 2% foaming gel and betamethasone dipropionate 0.05% lotion in the treatment of seborrhoeic dermatitis in adults. Dermatology. 1992; 184: 275–280.
12. Shuttleworth D, Squire RA, Boorman GC, Goode K. Comparative clinical efficacy of shampoos containing cliclopirox olamine (1.5%) or ketoconazole (2%; Nizoral®) for the control of dandruff/seborrhoeic dermatitis. J Dermatolog Treat. 1998; 9: 157-162.
13. Squire RA, Goode K. A randomised, single-blind, single-centre clinical trial to evaluate comparative clinical efficacy of shampoos containing ciclopirox olamine (1.5%) and salicylic acid (3%), or ketoconazole (2%, Nizoral) for the treatment of dandruff/seborrhoeic dermatitis. J Dermatolog Treat. 2002; 13: 51–60.
14. Lebwohl M, Plott T. Safety and efficacy of ciclopirox 1% shampoo for the treatment of seborrhoeic dermatitis of the scalp in the US population: results of a double-blind, vehicle-controlled trial. Int J Dermatol. 2004; 43(Suppl 1): 17–20.
15. Gupta AK, Bluhm R. Seborrheic dermatitis. J Eur Acad Dermatol Venereol. 2004; 18: 13–26.
16. Faergemann J. Management of seborrheic dermatitis and pityriasis versicolor. Am J Clin Dermatol. 2000; 1: 75–80.
17. Faergemann J. Seborrhoeic dermatitis and Pityrosporum orbiculare: treatment of seborrhoeic dermatitis of the scalp with miconazole-hydrocortisone (Daktacort), miconazole and hydrocortisone. Br J Dermatol. 1986; 114: 695–700.
18. Saple DG, Ravichandran G, Desai A. Evaluation of safety and efficacy of ketoconazole 2% and zinc pyrithione 1% shampoo in patients with moderate to severe dandruff — a postmarketing study. J Indian Med Assoc. 2000; 98: 810–811.
19. Lassus A, Nolting KS, Savopoulos C. Comparison of ciclopirox olamine 1% cream with ciclopirox 1%-hydrocortisone acetate 1% cream in the treatment of inflamed superficial mycoses. Clin Ther. 1988; 10: 594–599.
20. Rosen T, Schell BJ, Orengo I. Anti-inflammatory activity of antifungal preparations. Int J Dermatol. 1997; 36: 788–792.
21. Shuster S, Meynadier J, Kerl H, Nolting S. Treatment and prophylaxis of seborrheic dermatitis of the scalp with antipityrosporal 1% ciclopirox shampoo. Arch Dermatol. 2005; 141: 47–52.
22. Altmeyer P, Hoffmann K, Loprox Shampoo Dosing Concentration Study Group. Efficacy of different concentrations of ciclopirox shampoo for the treatment of seborrheic dermatitis of the scalp: results of a randomized, double-blind, vehicle-controlled trial. Int J Dermatol. 2004; 43(Suppl 1): 9–12.
23. Lee JH, Lee HS, Eun HC, Cho KH. Successful treatment of dandruff with 1.5% ciclopirox olamine shampoo in Korea. J Dermatolog Treat. 2003; 14: 212–215.
24. Van Cutsem J, Van Gerven F, Fransen J, Schrooten P. Janssen PA. The in vitro antifungal activity of ketoconazole, zinc pyrithione, and selenium sulfide against Pityrosporum and their efficacy as a shampoo in the treatment of experimental pityrosporosis in guinea pigs. J Am Acad Dermatol. 1990; 22: 993–998.
25. McGinley KJ, Leyden JJ. Antifungal activity of dermatological shampoos. Arch Dermatol. Res 1982; 272: 339–432.
26. Marks R, Pearse AD, Walker AP. The effects of a shampoo containing zinc pyrithione on the control of dandruff. Br J Dermatol. 1985; 112: 415–422.
27. Warner RR, Schwartz JR, Boissy Y, Dawson Jr. TL. Dandruff has an altered stratum corneum ultrastructure that is improved with zinc pyrithione shampoo. J Am Acad Dermatol. 2001; 45: 897–903.
28. Ware J, Kosinski M, Keller S. A 12-item short-form health survey. Construction of scales and preliminary tests of reliability and validity. Med Care. 1996; 34: 220–233.
29. Finlay AY, Khan GK. Dermatology Life Quality Index (DLQI) — a simple practical measure for routine clinical use. Clin Exp Dermatol. 1994; 19: 210–216.
30. Danby FW, Maddin WS, Margesson LJ, Rosenthal D. A randomized, double-blind, placebo-controlled trial of ketoconazole 2% shampoo versus selenium sulfide 2.5% shampoo in the treatment of moderate to severe dandruff. J Am Acad Dermatol. 1993; 29: 1008–1012.
31. Peter RU, Richarz-Barthauer U. Successful treatment and prophylaxis of scalp seborrhoeic dermatitis and dandruff with 2% ketoconazole shampoo: results of a multicentre, double-blind, placebo-controlled trial. Br J Dermatol. 1995; 132: 441–445.
32. Chosidow O, Maurette C, Dupuy P. Randomized, openlabeled, non-inferiority study between ciclopiroxolamine 1% cream and ketoconazole 2% foaming gel in mild to moderate facial seborrheic dermatitis. Dermatology. 2003; 206: 233–240.
33. Pierard-Franchimont C, Pierard GE, Arrese JE, De Doncker P. Effect of ketoconazole 1% and 2% shampoos on severe dandruff and seborrhoeic dermatitis: clinical, squamometric and mycological assessments. Dermatology. 2001; 202: 171–176.
[9738]
Другие материалы

Действие креатина и ацетила тетрапептида у женщин с острой телогеновой алопецией
Ранее проведенные исследования ex vivo на волосяных фолликулах выявили, что ацетил тетрапептид тормозит экспрессию гена TNF-α (фактор некроза опухоли альфа – ФНО-альфа) и что креатин индуцирует экспрессию белка NOGGIN. Подробнее

in vitro-исследование противогрибкового действия циклопироксоламина в отдельности и в комбинации с пиритионом цинка в сравнении с кетоконазолом в отношении стандартных штаммов микромицетов Malassezia globosa и Malassezia restricta

Оценка клинической эффективности применения шампуня, содержащего 1.5% циклопироксамина и 1% пиритион цинка, для устранения симптомов себорейного дерматита
В процессе исследования, в которое было включено 442 пациента с СД, была показана его высокая эффективность в отношении основных симптомов заболевания (уменьшение интенсивности эритемы на 93%, десквамации на 79%). В 94% случаев пациенты отмечали уменьшение субъективных ощущений (зуда). Подробнее
Комментарии
- Вконтакте